При оценке качества воды следует учитывать не только уровень жесткости и потенциал образования накипи, но также и коррозионные свойства, которые могут существенно повлиять на здоровье человека и функциональность оборудования. Тщательное исследование данных показателей позволяет выбрать целесообразный и действенный набор мер для эффективной очистки воды.
Норма жесткости воды для питья
Вода, будучи жизненно важным компонентом для нормального функционирования организма человека, крайне важна для поддержания здоровья. Однако природная H2O редко встречается в своем чистом виде; заместо этого уровень примесей варьируется в зависимости от конкретного источника. Содержание солей в водяном растворе играет ключевую роль в долговечности домашней техники и качества потребляемой воды.
Стандарты жесткости воды установлены для защиты здоровья населения и обеспечения надежности оборудования, используемого в различных сферах промышленного производства.
- Понятие жесткости воды
- Причины жесткости воды
- Типы жесткости воды
- Общая
- Временная (карбонатная)
- Постоянная (некарбонатная)
- Влияние жесткой воды на здоровье человека
- Нормы жесткости воды
- Для питьевой
- Для технической
- Расчет жесткости воды
- Способы определения уровня жесткости воды
- Методы устранения жесткости воды
- Катионирование
- Термоумягчение
- Реагентное умягчение
- Обратный осмос
- Электродиализ
- Дистилляция
- Дополнительная информация
Понятие жесткости воды
Вода может поступать как из открытых, так и из подземных источников. Почва, окружающая эти источники, насыщена разнообразными солями щелочноземельных элементов, в частности, кальция и магния (которые могут быть представлены в виде сульфидов, фторидов и других соединений). Уровень содержания этих солей в H2O определяет ее общую жесткость.

Причины жесткости воды
Степень жесткости воды в значительной мере определяется количеством растворенных в ней соединений. Главными факторами, способствующими высокой концентрации примесей, являются характер окружающей почвы и сезонные изменения. Например, H2O, формирующаяся в районах с высоким содержанием кальция, будет обогрена карбонатом кальция. В подземных водах рек или озер органические соединения и различные соли содержатся в значительных объемах, поскольку минералы и продукты разложения животных благоприятно влияют на обогащение водного раствора.
Лед, имеющий кристаллическую решетку, при замерзании воды обуславливает смещение инородных соединений. Концентрация солей зачастую оказывается выше зимой, чем весной, поскольку растаявший лед содержит небольшое количество примесей.
Как образуются соли жесткости
Вода известна как универсальный растворитель, в которой состав природных источников может значительно отличаться в зависимости от типа почвы. Например, H2O, обогащенная углекислым газом, проникает в почву и пронизывает слои геологических образований, таких как гипс, доломит, кальцит, смывая их и обогащая водный раствор органическими и неорганическими веществами, а также ионами различных металлов. Это вмешательство в свою очередь формирует минерализацию воды, известную как TDS (общее содержание растворенных веществ).
Преобладающими катионами в таких растворах являются катионы кальция и магния, а их комбинированный уровень определяет общую жесткость воды. Общая жесткость классифицируется на два основных типа:
- временная (карбонатная);
- постоянная (некарбонатная).
Формула для вычисления общей жесткости выглядит следующим образом:
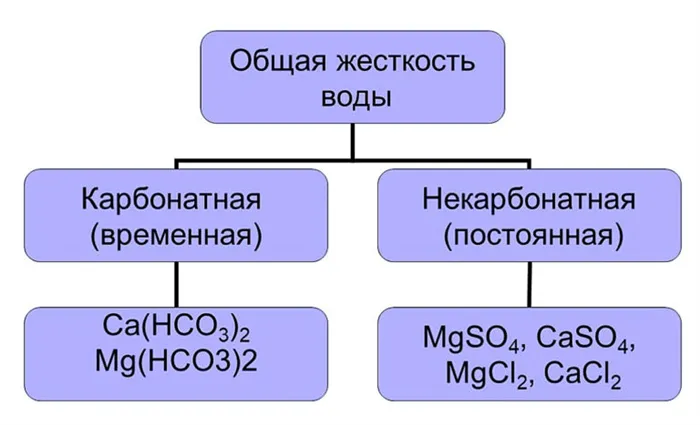
Карбонатная жесткость возникает из-за присутствия гидрокарбонатов Ca(HCO3)2 и Mg(HCO3)2, которые легко удаляются из раствора и создают нерастворимый осадок при нагревании. Второй вид жесткости, постоянная, определяется тем, что в воде находятся растворимые соли, которые не могут быть выведены из раствора путем нагрева. Для удаления постоянной жесткости применяются различные методы, которые описаны в следующих разделах статьи.
Что касается поверхностных вод, то в отличие от подземных источников, которые имеют более высокую концентрацию солей, они чаще разбавляются осадками, что приводит к непостоянной жесткости. Уровень её может достигать крайних значений в зимний период и снижаться во время весеннего разлива рек. В то же время, уровень жесткости в подземных водах остается более стабильным.
Единицы измерения
Концентрация солей в воде измеряется в миллиграмм-эквивалентах на литр: 1 мг-экв/л эквивалентен 20,04 мг Ca2+ и 12,16 мг Mg2+. В международной системе единиц (СИ) этот показатель выражается в молях на кубический метр (моль/м3). В России существует своя шкала жесткости, где 1 ºC соответствует 1 мг-экв/л или 0,5 ммоль/л.
В других странах также применяется система измерения жесткости, однако, со своими числовыми значениями:
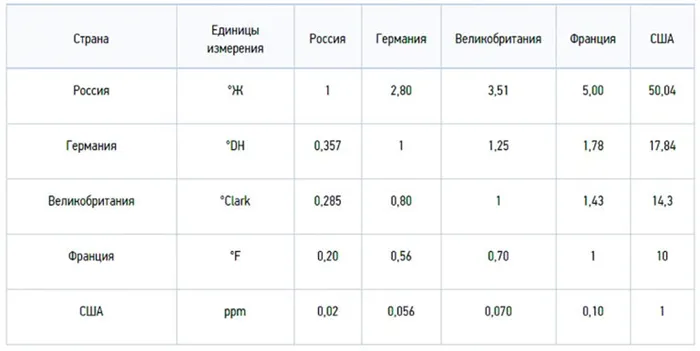
- В немецкой системе жесткости 1ºdH = 10 мг/л СаО или 7,194 мг/л MgO;
- Во французской системе 1ºfH = 10 мг/л СаСО3;
- В английской системе 1 ºClark = 14,254 мг/л СаСО3;
- В американской системе 1 gpg = 17,12 мг/л СаСО3.
Для упрощения перевода между различными единицами удобно применять такую американскую единицу, как PPM (parts per million), которая эквивалентна 1 мг/л CaCO3. Следовательно:
- 1ºdH = 17,9 ppm;
- 1ºfH = 10,0 ppm;
- 1 ºClark = 14,25 ppm;
- 1º gpg = 17,1 ppm;
- 1ºЖ = 50,05 ppm.
Для пересчета из промилле в градусы жесткости ºJ можно воспользоваться конвертерами. Таким образом, для переходов между градусами можно использовать следующую шкалу:
1 ºG = 2,804 ºdH = 3,5 ºClark = 5,005 ºfH = 2,924 gpg = 50,05ppm.
Нормы жесткости
Существует несколько классов жесткости воды, которые определяются по общему уровню твердости:
- мягкая – до 4 ºЖ;
- средней жесткости – от 4 до 8 ºЖ;
- жесткая – более 8 ºЖ.
Разнообразие природных условий в России делает невозможным установление единых стандартов жесткости воды для всех регионов. Это разнообразие сильно затрудняет создание универсальных рекомендаций.
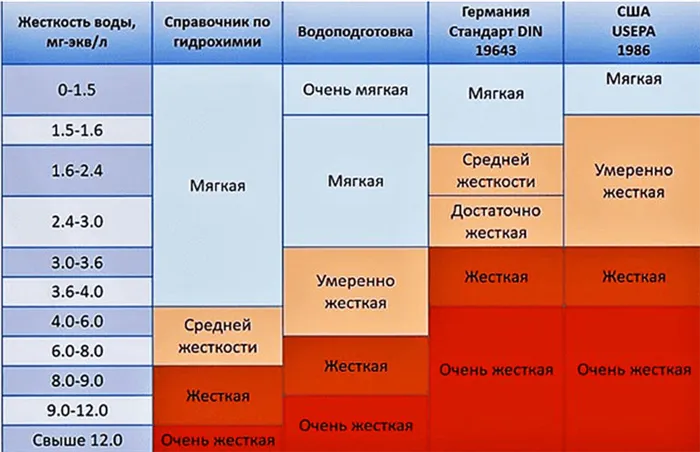
Тем не менее, предписанные стандарты для питьевой воды в целом согласуются с рекомендациями Всемирной организации здравоохранения (ВОЗ). В России действует ГОСТ 31954-2012, который представляет собой национальный стандарт c 01.01.2014. Данный стандарт учитывает ключевые международные рекомендации по качеству воды и методам ее анализа. Он применяется ко всем источникам как подземных, так и поверхностных вод.
Таблица 1. Нормальные значения концентрации кальция и магния в питьевой воде.
| № | Стандарт. | Продукт | Ca, мг/л | Mg, мг/л | Степень, ºДж |
|---|---|---|---|---|---|
| 1 | СанПин_2.1.4.1074-01, ГН_2.1.5.1315-03 | Питьевая вода | Не регламентируется | Не регламентируется | 7 |
| 2 | СанПин 2.1.4.1116-02 | Бутилированная вода | 25-130 | 5 — 65 | 1,5-7 |
| 3 | Нормы ВОЗ | Питьевая вода | 20-80 | 10 — 30 | Не предлагается |
Состав воды регулируется шкалой жесткости, которая зависит от ее назначения:
- допустимый уровень жесткости для водопроводной воды составляет 300 ppm или 6 ºЖ;
- оптимальные значения для природных водоемов колеблются в пределах 400 ppm или 8 ºЖ;
- предельно допустимый уровень жесткости не должен превышать 500 ppm, что соответствует 10 ºЖ;
- концентрация солей, становящаяся опасной для здоровья, определяется как более 500 ppm, т.е. >10 ºЖ.
К воде, впитывающей котлы электростанций, предъявляются особенно строгие требования — общее содержание жесткости не должно превышать 0,05-0,1 мг-экв/л.
Единицы измерения жесткости воды
Жесткость воды, в числовом выражении, обозначает концентрацию ионов кальция и магния. Хотя международная система единиц рекомендует измерять этот показатель в молях на кубический метр, на практике гораздо удобнее использовать альтернативные единицы.
В отечественной практике жесткость часто измеряется в градусах (1°Ж), где 1°Ж является эквивалентом миллиграмм-эквивалента на литр (мг-экв/л или мэкв/л).
- 1°Ж = 1 мг-экв/л. Для сравнения: 1°Ж = 2,8 dH (Германия).
- 1 мг-экв/л равен 20,04 мг Ca2+ или 12,16 мг Mg2+ в литре воды.
Таблица жесткости
| Природа воды | Жесткость в мг-экв/л | Степень dH |
|---|---|---|
| Очень мягкая | до 1,5 мг-экв/л | 0–4° |
| Мягкая | 1,5–3 мг-экв/л | 5–8° |
| Средней жесткости | 3–8 мг-экв/л | 9–12° |
| Жесткая | 8–12 мг-экв/л | 13–22° |
| Очень жесткая | выше 12 мг-экв/л | 23–34° |

Норма жесткости
Вода делится на три категории жесткости согласно градусам «природной» жесткости, ºЖ:
- мягкая: до 3°Ж;
- средняя по жесткости: 3–6°Ж;
- жесткая: более 6°Ж.
Согласно санитарным нормам, максимальная жесткость для водопроводной воды не должна превышать 7 мг-экв/л.
На практике, даже средняя жесткость может вызвать значительные неудобства. Например, жесткость в 4-5°Ж может привести к образованию накипи в чайниках и образованию пленки на напитках. Также это может вызвать накопление накипи на сантехнике, оставляющей белые следы на посуде, а также «засорять» сливные краны и душевые лейки.
Нормы жесткости для воды
Регулирование жесткости воды осуществляется через различные стандарты. Зачастую точные значения получают посредством анализов образцов в аккредитованных лабораториях и санитарно-эпидемиологических службах. Для регистрации анализов введены международные единицы измерения жесткости воды:
- моль/м3 — количество молей на кубический метр жидкости;
- мг-экв/л — миллиграмм-эквиваленты на литр;
- °Ж — градус жесткости.
Измеряемой единицей жесткости воды является 1 мг-экв/л, что соответствует половине миллилитра на литр. Допустимые значения для ионов кальция и магния разные: для Ca2+ 1°Ж = 20,04, для Mg2+ 1°Ж = 12,16 мг/л. Важно помнить, что эти значения используются при расчете жесткости, см. ниже в тексте.
Вода может быть мягкой, средней или жесткой. Мягкая вода включает в себя дистиллированную, кипяченую, дождевую и талую воду. Воду с умеренной жесткостью можно получить из централизированных систем водоснабжения. Артезианская и родниковая вода также имеют нормальны показатели. Вода из соленых водоносных горизонтов, которую необходимо подвергать опреснению, относится к высокожесткой.
Предельно допустимое содержание солей жесткости в воде
| Степень жесткости воды | Показатель в мг-экв/л | Показатель в °Ж | Показатель в ppm |
| Слишком мягкая | до 1,5 | до 1-1,5 | 0-70 |
| Мягкая | 1,5-4 | 1,6-4 | 71-140 |
| Среднежесткая | 5-8 | 5-12 | 141-210 |
| Сильножесткая | 9-12 | 13-22 | 211-320 |
| Сверхжесткая | свыше 12 | 23-34 | 321-530 |
Нормы жесткости для питьевой воды
СанПиН предлагает свои значения, которые колеблются в зависимости от назначения водных растворов. Жесткость воды по ГОСТ коррелируется в зависимости от типа и использования жидкости:
- Для обычной столовой водицы определяются значения концентрации магния (до 50 мг/л).
- В бутилированной учтены значения Ca = 25-130 и Mg = 5-65 мг/л.
- Для воды, предназначенной для хозяйственно-питевых нужд, ПДК питьевой воды не должно превышать 350 мг/л (7-10 мг-экв/л или 1-1,5 грамма на литр).
- Для товаров высшей категории допускается значение Жо=1,5-7, для первой – не более 7 мг-экв/л.
- Согласно нормам ВОЗ, в питьевой воде допускается 10-30 мг магния и 20-80 мг кальция на один литр.
- Общая жесткость для питьевой воды по EC не должна превышать 1,2 мг-экв/л.
Нижние пределы значений жесткости, применяемые в питьевой воде, устанавливаются из регламентированных норм. В обычной воде должно содержаться небольшое количество солей: кальций полезен организму, и его микроэлементы лучше усваиваются из напитков, чем из пищи. Требуемая массовая концентрация кальция в питьевой воде должна составлять не менее 0,12 мг/дм3, а магния – не менее 0,04. Хлористые и сульфатные соединения также должны присутствовать в количестве не менее 2 мг/дм3. Недостаток кальция в организме может привести к негативным последствиям, таким как разрушение костей и зубов, тогда как его избыток способен спровоцировать образование камней и привести к проблемам в работе выделительной системы.Активная и высокая соленость воды оказывает разрушительное воздействие на водопроводные системы, забивая стенки труб различными отложениями и увеличивая затраты на отопительные системы.
Если уровень содержания солей жесткости в воде превышает допустимые стандарты, ее необходимо очистить до приемлемого уровня. В таблице ниже приведены концентрации солей по шкале жесткости в промилле.
Шкала жесткости
| Концентрация солей | Величина в ppm (в промилле или мг/л) |
| Представляющая опасность для жизни | свыше 500 |
| Предельно допустимая | 500 |
| Средний показатель вод, добываемых из природных водоемов | 400 |
| Допустимое значение воды из водопровода | 300 |
| После прохождения угольных фильтров | 170 |
| После очистки системой обратного осмоса | 0-50 |
Нормы жесткости для технической воды
Определенные уровни жесткости воды, подходящие для котлов, устанавливаются отдельно в зависимости от уровня давления:
- до 1,4 МПа (14 кгс/см2) = 15-20;
- 2,4 МПа (24 кгс/см2) = 10-15;
- 3,9 Мпа (40 кгс/см2) = 4-10 мкмоль/дм3 (мкг-экв/дм3).
Первая (нижняя) цифра абсолютна для котлов, работающих на жидком топливе, с тепловым потоком более 350 кВт на квадратный метр, в то время как вторая (более высокая) цифра применяется к котлам, использующим другие источники топлива с более низким тепловым потоком, до 350 кВт/м2.
ГОСТ по определению жесткости воды указывает, какие параметры считаются допустимыми:
- для электронного производства,
- для гальваники,
- для энергетических систем,
- для медицинских процессов,
- для подпиточной и добавочной воды в котлах.
Разные степени жесткости питьевой воды распределяются отдельно: это может быть дистиллированная вода, водопроводная вода или бутилированная. Значения солей железа должны рассчитываться отдельно.
Как определить жесткость воды в лаборатории
Оптимальная степень жесткости воды является очень важной, так как нехватка солей может отрицательно сказаться на здоровье человека. Например, недостаток карбонатов в воде может привести к повышенному риску сердечно-сосудистых заболеваний.
Говоря о емкостях, в которых происходит нагрев воды, следует заметить, что мягкая вода может способствовать коррозии. Поэтому после работы методов с мягкой водой поверхности дополнительно обрабатываются раствором, содержащим замедляющие коррозию компоненты.
Следовательно, независимо от источника, из которого поступает вода, мы должны быть уверены в ее жесткости, которая в идеале должна находиться в среднем диапазоне, так как как избыток солей, так и их недостаток приводят к конечным негативным последствиям.

В наше время определить жесткость воды довольно просто. Вы можете приобрести специальное устройство для измерения жесткости как в домашних условиях, так и на рабочем месте. Наиболее популярное оборудование — прибор TDS-3, который можно найти на рынке под разными брендами.

Другой подходящий прибор для определения жесткости воды — электролит. Это устройство, как правило, не является сильно затратным.

Электролит не может дать точное численное значение жесткости воды, однако он способен окрасить жидкость в соответствии с содержанием солей. По интенсивности окраски после электролиза можно установить, какие именно примеси находятся в жидкости.
Вы также можете самостоятельно собрать подобное устройство, используя следующие материалы:
- лист нержавеющей стали, размером 50 х 50 см;
- болты М6 х 150;
- шайбы;
- гайки;
- прозрачную трубку;
- штуцеры;
- пластиковый контейнер объемом 1,5 литра;
- фильтр для очистки воды;
- обратный клапан для воды.
В качестве основы для вашего устройства можно использовать лист нержавеющей стали, предпочтительно AISI 316L для импортных и 03Х16Н15М3 для отечественных. Теперь необходимо разметить и нарезать его на 16 квадратов одинакового размера. У каждого квадрата обрежьте угол и просверлите в противоположном углу отверстие, которое потребуется на следующем этапе.
Работа электролита основывается на передаче электричества от одного электрода к другому, расщепляя воду на кислород и водород. Пластины должны быть подключены поочередно: сначала положительная зарядка, затем отрицательная, потом снова положительная и так далее. Для междуэлементной изоляции используется трубка, из которой вырезается кольцо для создания полосы толщиной в 1 мм.
Для сборки пластин необходимы шайбы: одна шайба навинчивается на болт, далее устанавливается деревянная пластина, после этого три шайбы под одну и так до конца, чередуя с каждой пластиной, таким образом в каждом элементе должно быть восемь пластин. Важно делать это аккуратно, чтобы избежать касания пластин между собой.
Как определить жесткость воды с помощью мыла
Этот метод, описанный И. Шереметьевым, основывается на том, что для образования пены мыло требуются определенные условия, и в жесткой воде мыло с трудом вспенивается из-за избытка солей кальция и магния.
Для определения жесткости воды воздухом, возьмите 1 г обычного стирального мыла, разделите его на мелкие кусочки и медленно растворите в небольшом объеме горячей дистиллированной воды, избегая образованию пены.
Перелив полученного раствора в цилиндрический стакан, добавьте дистиллированную воду до уровня 6 см для мыла с содержанием 60% или до уровня 7 см для 72% (целевой процент будет указан на упаковке мыла). Каждый см раствора будет соответствовать количеству мыла, необходимому для связывания солей жесткости: 1 dH на 1 литр жидкости. Теперь заполните литровую емкость наполовину водой с неизвестной жесткостью, взбалтывая содержимое стакана, добавляя постепенно полученный раствор. Вначале могут появиться небольшие темные хлопья, а затем образуются пузырьки. Если появляется густая белая пена, это означает, что все соли жесткости были связаны в исследуемой жидкости. Подсчитайте, сколько сантиметров приготовленного раствора вы добавили – каждый сантиметр отвечает за содержание солей в 0,5 литра воды, что соответствует 2°dH. Например, если чтобы получить пену потребовалось добавить 4 см мыльного раствора, это обозначает, что жесткость воды составляет 8°dH.
Если раствор готов, но пена не образуется, значит, жесткость превышает 12°dH. Чтобы выявить точное значение, повторите тест, дважды разбавив пробу дистиллированной водой. Результат повторного теста необходимо удвоить, чтобы получить значение жесткости воды.
Обычно стандартные стаканы имеют размеры: объем 200-250 мл, высота 10 см, диаметр дна 55 мм или более, верхний диаметр 73 мм. Таким образом, средний диаметр составляет около 63 мм. Более точно определять жесткость можно с помощью цилиндрического стакана диаметром около 6 см. Также можно использовать коническую чашу, но в этом случае погрешность будет больше. Следует заметить, что точность метода не слишком велика, однако составляет относительно приемлемое значение в 1-2 °dH, что достаточно для уровня оценки состояния жидкости. Погрешность метода во многом объясняется разницей в диаметр верхней и нижней части ёмкости с раствором, а также качеством мыла, дистиллированной жидкости и вашим опытом выполнения анализа.
Этот метод является простым и позволяет определить жесткость воды самостоятельно, небольшой уровень погрешности не должен останавливать вас от его использования.
Как еще определить жесткость воды в домашних условиях
Определить жесткость воды на самом деле не так сложно. Если вам потребуются точные данные, вы всегда можете отправить образец в специализированную лабораторию для анализа. Для этого есть множество современных методов. Наилучший способ — использовать реагент Trilon B для тестирования жесткости. Для получения оперативных результатов можно использовать специальное оборудование, стоимость которого начинается с 10-15 у.е. Это достаточно небольшая сумма, учитывая, что вам периодически может потребоваться контроль жесткости воды.
Если нет необходимого прибора, но вам срочно нужно узнать уровень жесткости воды, можете воспользоваться следующим методом. Простой способ — умыться с использованием бруска мыла: если пена не образуется и кожа становится сухой, а на душевой лейке или чайнике появляется налет, значит, речь идет о жесткой воде. Если же пена образуется, то вода мягкая или имеет среднюю жесткость.
Существует и множество других методов для определения уровня жесткости:
- Определить качество воды можно по ее внешнему виду и вкусу. Идеально, если жидкость прозрачная и не содержит осадка, и не обладает посторонними запахами.
- Чтобы установить чистоту воды, налейте ее в прозрачный чистый стакан на 20 см и поставьте на текст с печатным текстом. Если текст можно прочитать, значит, вода соответствует нормам.
- Вы можете также оценить цвет воды в том же стакане, но налив 100 мл воды. После этого вставьте стакан на белую поверхность. Наличие органических примесей придаст воде темный оттенок.
- Запах тоже может сказать много о качестве жидкости. Подогрейте воду сначала до 20°С, а затем до 60°С. Если ощущается неприятный гнилостный запах, значит, в воде имеются примеси сероводорода.
- Вкус также может свидетельствовать о качестве. Налейте воду в чистую емкость, прокипятите небольшую порцию воды в течение 5 минут и остудите до 20°С–25°С, после чего попробуйте. Сладковатый вкус указывает на присутствие гипса, горький – на соли магния, терпкий – на соли железа. Гнилостный привкус может появиться из-за попадания растительных или животных примесей. Процесс фильтрации может помочь определить наличие твердых частиц, но предварительно стоячая вода должна отстояться в течение какого-то времени.
- Попробуйте капнуть воду на стекло или зеркало. После испарения жидкости внимательно осмотрите поверхность: если она чистая, вода также удовлетворительная. Наличие пятен – явный признак плохого качества жидкости. Если есть аквариум, попробуйте изучить поведение его обитателей – они очень чувствительны к свойствам воды.
Несмотря на разнообразие предложенных методов, ни один из них не дает точного значения жесткости и качества воды, поэтому в ситуациях, когда требуется высокая точность своих данных, следует обратиться к профессионалам.
Безусловно, когда вы проводите тестирование жесткости воды в своей квартире, дому или на даче, лучше воспользоваться высокоспециализированными тестами, поскольку количества магния и кальция в воде могут значительно варьироваться в зависимости от множества факторов.
Хотя на тестирование может уйти значительная сумма, вы будете уверены, насколько эффективен ваш фильтр для воды.
На рынке представлено множество российских компаний, которые разрабатывают различные системы очистки воды. Если вы будете полагаться только на свои знания, не всегда можно выбрать подходящий фильтр. Создание системы очистки воды в домашних условиях, даже с предварительной подготовкой, может оказаться не самым эффективным способом очистки.
Это, разумеется, путь, но не всегда безошибочный и верный. Для достижения хороших результатов лучше следовать проверенным рекомендациям и системам.